高一
我能力有限,自己翻講義獲得的會比這網頁多
1.物質組成
1-1.1純物質與混合物
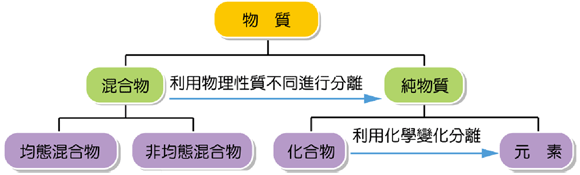
1-1.2物質狀態
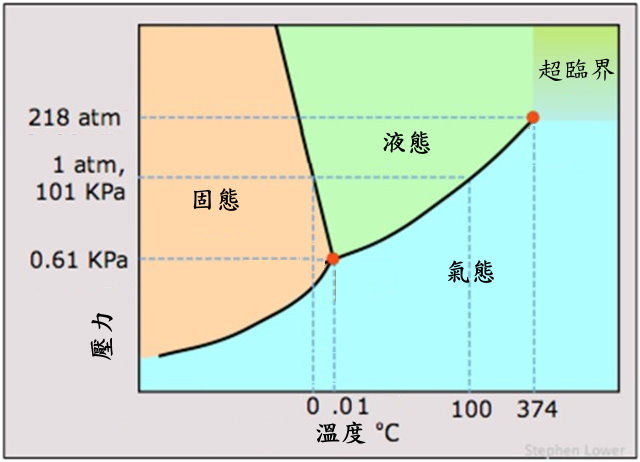
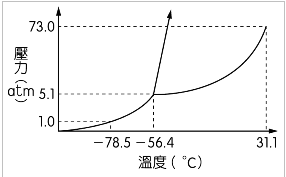
- 上方這張是水的相圖
- 固液共存線斜率為負
- 通常相圖繪相下方這張斜率為正
1-1.3混合物的分離
- 蒸餾:物質的沸點溫度差
- 萃取:物質的溶解度差
- 色層分析:不同物質的附著力差
- 過濾:物質粒徑大小
- 結晶:加熱後晶體析出
- 傾析:利用比重不同倒出
1-2道耳頓原子說
1.定比定律
化合物組成的元素間有一定的質量比
ex:H2O質量比恆為1:8
2.倍比定律
如果兩種元素可以生成兩種元素以上的化合物,在這些化合物中,將其中一個元素的質量固定,則另一元素質量成簡單整數比

3.原子說
| 道耳頓 | 現今 |
|---|---|
| 不可分割原子 | 原子由e,p,n組成 |
| 相同元素及原子有相同的質量與性質 | 發現同位素的存在 |
| 化合物->簡單整數比 | 晶體有缺陷時原子比例常違背 |
| 化學反應發生時原子會重新排列組合 | 物理/化學反應無法產生新原子,but核反應可以 |
4.亞佛加厥定律
- 在相同溫度及壓力下,相同體積的任何氣體其分子數目相同
- 氣體分子由數個[原子]組成
5.莫耳數 - 1mole=1亞佛加厥常數=6.02*1023
- mole是數量單位
1-4原子結構與元素週期表
重點:
e與p的W差了約1800倍
2.元素週期表

- 依原子序排 橫排叫列or週期
- 1A為鹼金屬,2A為鹼土金屬,7A為鹵素,8A為鈍氣
- B族金屬稱過度元素
3.電子殼層與能階

| 由左往右 | 由上往下 |
|---|---|
| 原子半徑/金屬特性變小 | 原子半徑/金屬特性變大 |